I’m a passionate writer who loves exploring ideas, sharing stories, and connecting with readers through meaningful content.I’m dedicated to sharing insights and stories that make readers think, feel, and discover something new.
1. घटना की शुरुआत और जांच की तारीखें
5 अक्टूबर 2025: मध्य प्रदेश के छिंदवाड़ा और सिवनी जिलों में एक के बाद एक बच्चों की तबीयत बिगड़ने लगी। सभी में उल्टी, बेहोशी और गुर्दे फेल होने जैसे लक्षण पाए गए।
अस्पतालों में भर्ती बच्चों में से कई ने दम तोड़ दिया। कुल 19 बच्चों की मौत 5 से 8 अक्टूबर 2025 के बीच हुई।
स्वास्थ्य विभाग ने मृत बच्चों के परिवारों से पूछताछ की तो पाया कि सभी को एक ही दवा – Coldrif Cough Syrup – दी गई थी।
7 अक्टूबर 2025: राज्य दवा नियंत्रण विभाग ने उस दवा के सैंपल एकत्र कर Bhopal की प्रयोगशाला भेजे।
8 अक्टूबर 2025: प्राथमिक रिपोर्ट में पता चला कि सिरप में Diethylene Glycol (DEG) की मात्रा बहुत अधिक थी — यह एक औद्योगिक केमिकल है जो शरीर में जाकर किडनी फेलियर और मौत का कारण बन सकता है।
9 अक्टूबर 2025: भारत सरकार के स्वास्थ्य मंत्रालय ने आधिकारिक रूप से तीन खांसी की दवाओं (Coldrif, Respifresh TR, ReLife) को “विषाक्त (Toxic)” घोषित किया।
10 अक्टूबर 2025: विश्व स्वास्थ्य संगठन (WHO) ने भी अंतरराष्ट्रीय चेतावनी (Global Alert) जारी की कि भारत में बनी ये दवाएँ बच्चों के लिए घातक हैं।
13 अक्टूबर 2025: भारत की जांच एजेंसी (Central Crime Bureau) और मध्य प्रदेश पुलिस ने चेन्नई स्थित Sresan Pharma के कारखाने और दफ्तरों पर छापेमारी की।
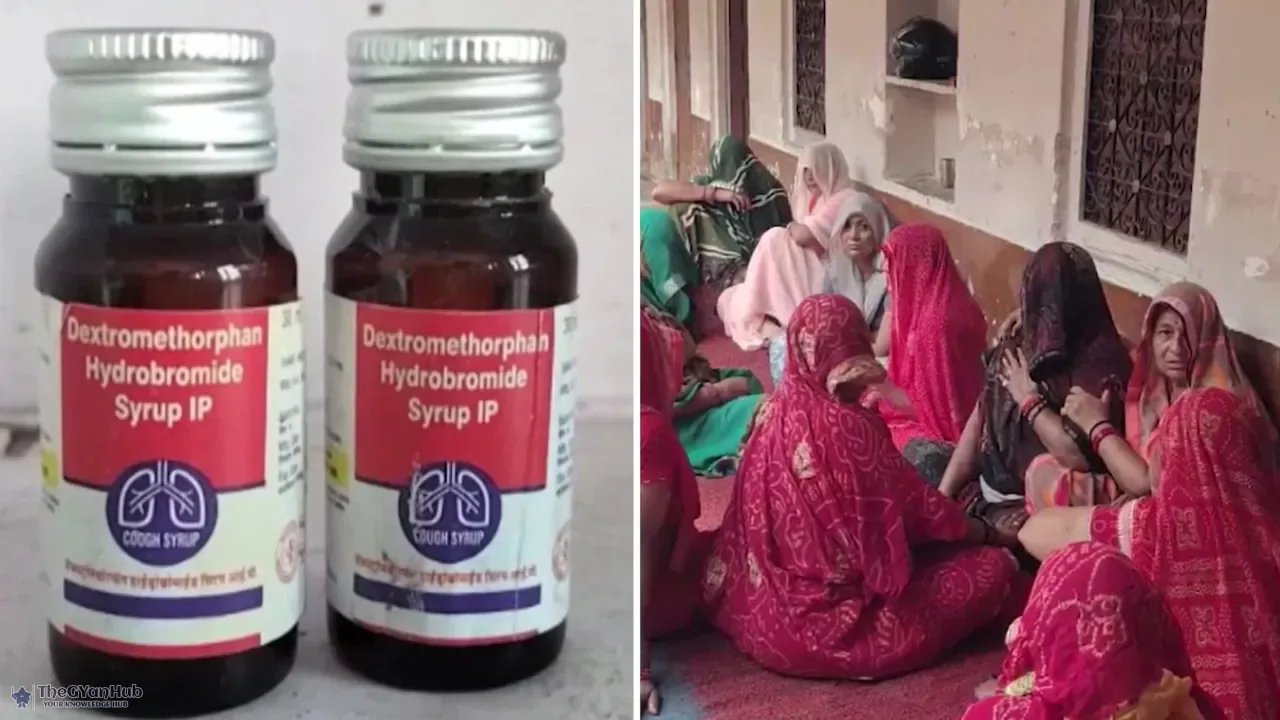
2. दवा में पाए गए घातक तत्व और नियमन की खामियाँ
जहरीला तत्व Diethylene Glycol (DEG)
DEG आमतौर पर औद्योगिक उत्पादों जैसे एंटीफ्रीज़ या पेंट में उपयोग होता है।
दवा निर्माण में इसे कभी भी मानव उपभोग के लिए उपयोग नहीं किया जाना चाहिए, लेकिन परीक्षणों में पाया गया कि Coldrif में 48.6% तक DEG था — जो अनुमेय सीमा (0.1%) से लगभग 500 गुना अधिक है।
यही रसायन किडनी फेलियर, ब्रेन डैमेज और मौत का कारण बनता है।
इसी तरह, Respifresh TR में 1.34% और ReLife Syrup में 0.61% DEG पाया गया, जो कि बच्चों के लिए घातक मात्रा है।
दवा नियमन में गंभीर चूकें
भारत में हर दवा निर्माता को प्रत्येक बैच की गुणवत्ता रिपोर्ट ड्रग्स कंट्रोलर को देनी होती है।
Sresan Pharma ने कई बैचों का परीक्षण या रिपोर्टिंग नहीं की।
कंपनी ने सस्ता औद्योगिक सॉल्वेंट उपयोग कर लागत घटाई, जिससे दवा जहरीली बन गई।
WHO और Indian Drug Regulatory Authority दोनों ने माना कि गुणवत्ता नियंत्रण में कई स्तरों पर लापरवाही हुई।
यह मामला गाम्बिया (2022) और उज़्बेकिस्तान (2023) में हुई भारत निर्मित सिरप से मौतों जैसी घटनाओं की याद दिलाता है।
3. कानूनी कार्रवाई, असर और भविष्य की चुनौतियाँ
कानूनी कार्रवाई और गिरफ्तारियाँ
13 अक्टूबर 2025: छापेमारी के दौरान Sresan Pharma के मालिक G. Ranganathan को पुलिस ने गिरफ्तार किया।
उनके खिलाफ IPC की धारा 304 (गैर इरादतन हत्या), धारा 274 (जहरीली दवा बेचना) और धारा 276 (मिलावटी दवा निर्माण) के तहत मामला दर्ज किया गया।
कंपनी का निर्माण लाइसेंस तत्काल रद्द किया गया और फैक्ट्री सील कर दी गई।
ED (Enforcement Directorate) ने भी मनी लॉन्ड्रिंग के एंगल से जांच शुरू की।
पंजाब, महाराष्ट्र और उत्तर प्रदेश ने Sresan Pharma की सभी दवाओं की बिक्री पर प्रतिबंध लगा दिया है।
समाज पर प्रभाव और जन प्रतिक्रिया
इस त्रासदी में जिन 19 बच्चों की मौत हुई, वे 2 महीने से 5 साल की उम्र के थे।
माता-पिता ने सरकार से मुआवज़ा और कड़ी सजा की मांग की।
सोशल मीडिया पर #JusticeForChildren और #BanToxicSyrups जैसे हैशटैग ट्रेंड करने लगे।
डॉक्टरों ने चेताया कि अब लोग किसी भी “सस्ती खांसी की दवा” को बिना ब्रांड जांचे न खरीदें।
स्वास्थ्य व्यवस्था के लिए सबक
दवा निर्माण की हर फैक्ट्री में रियल-टाइम टेस्टिंग लैब होना अनिवार्य किया जाना चाहिए।
राज्यों को अपने ड्रग कंट्रोल ऑफिस को मजबूत करना होगा — ताकि छोटे निर्माता बिना जांच के दवाएँ न बेच सकें।
सरकार को “दवा ट्रैकिंग सिस्टम” लागू करना चाहिए, जिससे हर बैच की जानकारी उपभोक्ता QR कोड से देख सके।
WHO ने सुझाव दिया कि भारत को अपनी दवा निर्यात प्रणाली की भी समीक्षा करनी चाहिए क्योंकि ऐसी घटनाएँ वैश्विक स्तर पर देश की छवि को प्रभावित करती हैं।
Related articles in this category

Rahul Khona Returns to Starbucks India as Chief Technology Officer
May 11, 2026
Rahul Khona has made a significant return to Starbucks India as the Chief Technology Officer, bringing a wealth of experience to enhance the brand's technological advancements.

Analysis: In Vijay's Delicate Coalition Tango, DMK Holds Some Strings
May 10, 2026
This article delves into the intricate dynamics of the coalition led by Vijay, highlighting the pivotal role played by the DMK amidst ongoing political maneuvers in Tamil Nadu.

Amazon Embraces AI for Hiring Surge Ahead of Festival Season
April 29, 2026
Amazon is leveraging artificial intelligence to streamline its hiring process in anticipation of the upcoming festival rush. The company has also introduced a new AI design philosophy to enhance its operational efficiency.






